Cho 4,72g hỗn hợp A gồm Fe, FeO, Fe2O3, tác dụng với CO dư (to cao) thu được 3,92g Fe. Cũng cho 4,72g A trên dung dịch CuSO4 dư, sau phản ứng được 4,96g chất rắn. Tính % khối lượng mỗi chất trong A. (Biết các phản ứng xảy ra hoàn toàn)

Những câu hỏi liên quan
Ống chứa 4,72g hỗn hợp Fe, FeO, Fe2O3 được đốt nóng rồi cho dòng H2 đi qua đến dư. Sau phản ứng trong ống còn lại 3,92g Fe. Nếu cho 4,72g hỗn hợp ban đầu vào dung dịch CuSO4 và lắc kỹ để phán ứng hoàn toàn, lọc lấy chất rắn, làm khô cân nặng 4,96g. Tính khối lượng từng chất trong hỗn hợp.
phương trình phản ứng
FeO + H2 = Fe + H2O (1)
y y mol
Fe2O3 + 3H2 = 2Fe + 3H2O (2)
z 2z mol
Fe + CuSO4(dung dịch pha loãng) = FeSO4 + Cu↓ (3)
x x mol
theo phương trình phản ứng (3) áp dụng định luật thay đổi khối lhuowngj ta có 64x - 56x = 4,96 - 4,72 => x=0,03 mol
khối lượng của Fe là mFe = 0,03.56=1,68(g)
khối lượng của oxit sắt còn lại là 3,04 g
theo bài ra ta có phương trình
72y + 160z = 3,04
56y + 56.2z = 3,92 - 1,68
giải hệ phương trình ta có y= 0,02 z= 0,01
còn lại khối lượng bạn tự tính nha![]()
Đúng 0
Bình luận (2)
Ống chứa 4,72g hỗn hợp Fe, FeO, Fe2O3 được đốt nóng rồi cho dòng H2 đi qua đến dư. Sau phản ứng trong ống còn lại 3,92g Fe. Nếu cho 4,72g hỗn hợp ban đầu vào dung dịch CuSO4 và lắc kỹ để phán ứng hoàn toàn, lọc lấy chất rắn, làm khô cân nặng 4,96g. Tính khối lượng từng chất trong hỗn hợp.
Cho 4,72 gam hỗn hợp bột gồm các chất Fe, FeO và Fe2O3 tác dụng với CO ở nhiệt độ cao. Phản ứng xong thu được 3,92 gam Fe. Nếu ngâm cùng lượng hỗn hợp các chất trên trong dung dịch CuSO4 dư, phản ứng xong khối lượng chất rắn thu được là 4,96 gam. Khối lượng (gam) Fe, Fe2O3 và FeO trong hỗn hợp ban đầu lần lượt là A. 1,68; 1,44; 1,6 B. 1,6; 1,54; 1,64 C. 1,6; 1,44; 1,64 D. 1,68; 1,6; 1,44
Đọc tiếp
Cho 4,72 gam hỗn hợp bột gồm các chất Fe, FeO và Fe2O3 tác dụng với CO ở nhiệt độ cao. Phản ứng xong thu được 3,92 gam Fe. Nếu ngâm cùng lượng hỗn hợp các chất trên trong dung dịch CuSO4 dư, phản ứng xong khối lượng chất rắn thu được là 4,96 gam. Khối lượng (gam) Fe, Fe2O3 và FeO trong hỗn hợp ban đầu lần lượt là
A. 1,68; 1,44; 1,6
B. 1,6; 1,54; 1,64
C. 1,6; 1,44; 1,64
D. 1,68; 1,6; 1,44
Đáp án D
Các phản ứng xảy ra:
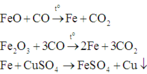
Hỗn hợp rắn thu được khi cho hỗn hợp phản ứng với dung dịch CuSO4 gồm Cu, FeO và Fe2O3.
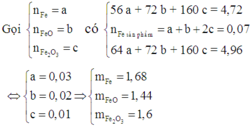
Đúng 0
Bình luận (0)
Cho 4,72 g hỗn hợp A (Fe,FeO,Fe2O3) tác dụng CO dư ở nhiệt độ cao thu được 3,92 g Fe .Cũng hỗn hợp trên tác dụng dung dịch CuSO4 dư trở thành 4,96g chất rắn .Tính khối lượng mỗi oxit trong hỗn hợp.
gọi x, y, z lần lượt là số mol của Fe, FeO, Fe2O3
theo bài ra ta có: 56*x+ 72*y + 160* z= 4.72 (g)
bảo toàn khối lượng ta có
nFe sau pứ = nFe ban đầu + nFeO + 2*nFe2O3
= x + y + 2*z =3.92/56=0.07(2)
ta có nCu = nFe = x
ta có 64*x + 72*y + 160*z = 4.96(3)
từ 1,2,3 ta có
x=0.03==> mFe = 56*0.03=1.68(g)
y=0.02==> mFeO = 72*0.02= 1.44(g)
z=0.01==>mFe2O3= 0.01*160=1.6(g)
Đúng 0
Bình luận (0)
Giúp mình nhé mấy bạn mình cần gấp nhak
Cho dòng khí H2 dư đi qua 3,54 gam hỗn hợp gồm Fe,FeO,Fe2O3 được đốt nóng sau khi phản ứng xong còn lại 2,94 gam Fe nếu cho 3,54 gam hỗn hợp ban đầu trên tác dụng với dung dịch CuSO4 cho đến khi phản ứng xảy ra hoàn toàn lọc lấy chất rắn sau khi làm khô chất rắn cân nặng 3,72 gam tính khối lượng của mỗi chất trong hỗn hợp ban đầu
FeO + CO -> Fe + CO2
mol: x -> x
pt2: Fe2O3 + CO ->2 Fe + CO2
mol: y -> 2y
theo gt thu được 2.94 g
Fe trong đó có Fe tạo thành và Fe ban đầu và gọi Z là số mol Fe ban đầu
=> ta có Pt : 72x + 160y +56z=3.54 (1)
và x + 2y + z =3.92/56=0.0525 (2)
hh trên vào CuSO4 thì chỉ có Fe phản ứng
pt: Fe + CuSO4 -> FeSO4 + Cu
mol: z -> z
thu được 3.72g rắn gồm Cu , FeO, Fe2O3
=> ta có pt: 72x + 160y + 64Z=3.72 (3)
từ (1),(2),(3) ta có x=0.015= nFeO , y=0.0075 mol =nFe2O3 , z=0.0225 mol=nFe
Có số mol áp dụng công thức m=n*M em tự tính khối lượng các chất nha
Số ko đẹp lắm nên số mol hơi dài,cứ giữ nguyên để tính để tránh sai số
CHÚC EM HỌC TỐT !!!!!!(nhớ hậu tạ nha hi hi.....)
Đúng 0
Bình luận (0)
Cho 4,8 gam hỗn hợp gồm Fe và Fe2O3 tác dụng với dung dịch CuSO4 dư. Phản ứng xong lấy chất rắn ra khỏi dung dịch rồi cho tác dụng với dung dịch HCl 1M thì còn 3,2 gam chất rắn màu đỏ.
a. Tính khối lượng mỗi chất trong hỗn hợp ban đầu.
b. Xác định thể tích dung dịch HCl đã dùng.
Đặt \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Fe_2O_3}=y\left(mol\right)\end{matrix}\right.\Rightarrow56x+160y=4,8\left(1\right)\)
\(PTHH:Fe+CuSO_4\rightarrow FeSO_4+Cu\\ \Rightarrow n_{Cu}=n_{Fe}=a\left(mol\right)\\ Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\\ Cu+2FeCl_3\rightarrow CuCl_2+2FeCl_2\\ \Rightarrow n_{Cu}=\dfrac{1}{2}n_{FeCl_3}=n_{Fe_2O_3}=b\left(mol\right)\\ \Rightarrow n_{Cu\left(dư\right)}=a-b=\dfrac{3,2}{64}=0,05\left(mol\right)\left(2\right)\)
\(\left(1\right)\left(2\right)\Rightarrow\left\{{}\begin{matrix}a=\dfrac{8}{135}\\b=\dfrac{1}{108}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}\%_{Fe}=\left(\dfrac{8}{135}\cdot56\right):4,8\cdot100\%\approx69,14\%\\\%_{Fe_2O_3}\approx30,86\%\end{matrix}\right.\)
\(b,n_{HCl}=6n_{Fe_2O_3}=\dfrac{1}{18}\approx0,06\left(mol\right)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,06}{1}=0,06\left(l\right)\)
Đúng 2
Bình luận (0)
Cho dòng khí H2 dư đi qua 3,54 gam hỗn hợp gồm Fe, FeO, Fe2O3 được đốt nóng sau khi phản ứng xong còn lại 2,94 gam Fe. + Nếu cho 3,54 gam hỗn hợp ban đầu trên tác dụng với dung dịch CuSO4 cho đến khi phản ứng xảy ra hoàn toàn lọc lấy chất rắn sau khi làm khô chất rắn cân nặng 3,72 gam tính khối lượng của mỗi chất trong hỗn hợp ban đầu
Xem chi tiết
\(FeO+H_2\underrightarrow{t^o}Fe+H_2O\)
y y
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
z 2z
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
x x
gọi x, y, z là số mol của Fe bđ, FeO bđ, \(Fe_2O_3bđ\)
có: \(\left\{{}\begin{matrix}56x+56y+\left(56.2\right)z=2,94\\56x+72y+160z=3,54\\64x+72y+160z=3,72\end{matrix}\right.\)
Giải được:
x = 0,0225
y = 0,015
z = 0,0075
=> m Fe bđ = 0,0225 . 56 = 1,26 (g)
m FeO bđ = 0,015.72 = 1,08 (g)
m \(Fe_2O_3\) bđ = 0,0075 . 160 = 1,2 (g)
( Với hệ pt:
- ở dòng 1, 56x, 56y, 112z là của pt Fe không td vs H2, pt FeO bị H2 khử và pt \(Fe_2O_3\) bị \(H_2\) khử.
- ở dòng 2, 56x: m Fe bđ
72y: m FeO bđ
160z: m \(Fe_2O_3\) bđ
- ở dòng 3, 64x: \(m_{Cu}\) khi Fe td với \(dd.CuSO_4\) tạo được x mol Cu
72y: m FeO không td với dd CuSO4
160z: m \(Fe_2O_3\) không td với dd \(CuSO_4\) )
Đúng 1
Bình luận (0)
Cho 8 gam hỗn hợp A gồm Mg và Fe tác dụng hết với 200 mL dung dịch CuSO4 đến khi phản ứng kết thúc, thu được 12,4 gam chất rắn B và dung dịch D. Cho dung dịch D tác dụng với dung dịch NaOH dư, lọc và nung kết tủa ngoài không khí đến khối lượng không đổi thu được 8 gam hỗn hợp gồm 2 oxit.Khối lượng Mg và Fe trong A lần lượt là A. 4,8 g và 3,2 g B. 3,6 g và 4,4 g C. 2,4 g và 5,6 g D. 1,2 g và 6,8 g
Đọc tiếp
Cho 8 gam hỗn hợp A gồm Mg và Fe tác dụng hết với 200 mL dung dịch CuSO4 đến khi phản ứng kết thúc, thu được 12,4 gam chất rắn B và dung dịch D. Cho dung dịch D tác dụng với dung dịch NaOH dư, lọc và nung kết tủa ngoài không khí đến khối lượng không đổi thu được 8 gam hỗn hợp gồm 2 oxit.Khối lượng Mg và Fe trong A lần lượt là
A. 4,8 g và 3,2 g
B. 3,6 g và 4,4 g
C. 2,4 g và 5,6 g
D. 1,2 g và 6,8 g
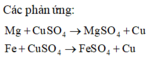
Dung dịch D gồm MgSO4 và FeSO4. Chất rắn B bao gồm Cu và Fe có thể dư
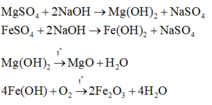
Gọi x, y là số mol Mg và Fe phản ứng. Sự tăng khối lượng từ hỗn hợp A (gồm Mg và Fe) so với hỗn hợp B (gồm Cu và Fe có thể dư) là
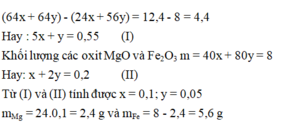
Đáp án C
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 57,6 gam hỗn hợp gồm fe3o4, fe203, feo, fe vào dung dịch hcl cần 360 gam dung dich hcl 18,25% để tác dụng vừa đủ . Sau phản ứng thu đươc V(l) h2 và dung dich b.a)Cho toàn bộ h2 sinh ra tác dụng với cuo dư ở nhiệt độ cao thu được hỗn hợp chất rắn có khối lương nhỏ hơn khối lượng cuo ban đầu là 3,2 gam a, nếu cô cạn dung dịch b thì thu bao nhiêu gam muối khan b,b)nếu hỗn hợp a ban đầu có tỉ lệ mol n(fe2o3) : n ( feo) 1: 1. Tính C% các chất trong dung dich bc)hỗn hợp x cũng chứa...
Đọc tiếp
Hòa tan hoàn toàn 57,6 gam hỗn hợp gồm fe3o4, fe203, feo, fe vào dung dịch hcl cần 360 gam dung dich hcl 18,25% để tác dụng vừa đủ . Sau phản ứng thu đươc V(l) h2 và dung dich b.
a)Cho toàn bộ h2 sinh ra tác dụng với cuo dư ở nhiệt độ cao thu được hỗn hợp chất rắn có khối lương nhỏ hơn khối lượng cuo ban đầu là 3,2 gam a, nếu cô cạn dung dịch b thì thu bao nhiêu gam muối khan b,
b)nếu hỗn hợp a ban đầu có tỉ lệ mol n(fe2o3) : n ( feo) = 1: 1. Tính C% các chất trong dung dich b
c)hỗn hợp x cũng chứa Fe3O4 ; Fe2O3 ; FeO ; Fe nếu dùng 100g (x ) cho tác dugnj với 2 lít dd hcl 2M . chứng minh rằng hỗn hợp x tan hết



















